| ������|�й��������̨|��վ��ͼ |
| �ͷ���Ϊ��ҳ |
��̸ | ֱ�� | �㳡 | ����ǽ | ���а�
• ���Ӵ��������ʶ�� • ���ؼ�ʮ����ȫ����
������Ŀ|
̽��������|
�ټҽ�̳|
������Ȼ|
����|
���
ԭ�����|��������|�����й�|��Ȼ����
��ѧ���磨��ͣ����| �ٿ�̽�أ���ͣ����| ���´��| �Ƽ�����
�߱��й�| �߽���ѧ| ��ɫ�ռ�| �Ƽ�֮��
�Ƽ�����| ��������| �л�����| ����
��֤������| ��֤��Ӱ��־| �ط�| ��֤������֮��
������| ������̸¼| ˿·����| �����DZ���
��������| �����ձ�| ��������| �����л���
�����й�| ����| ����֮��ɫ����| ��ת����
ֲ��|����|��ս|����|����|����|ʷ˵����|���ĵ���|�ܵ�|ʱ��|����̽��|�й��ʵ�|���պ���|��Ȥ|��ÿƼ�|�峯|��ʷʱ��|������|UFO|�Ļ�����|��¥��|����|����|�ղ�|��������|Ů��Ů��|Ů��|�Ƶ�|����|�˶�|��Դ����|����|��������|����|��������|����|��ʷ����|�ڽ�|����̽��|����|ר��|����|��ѧ̽��|�������|δ��֮��|����|����|����|���Ҵ�ʦ|����Ѱ��|��������|ս��|��Ȼ����|��ѧ|��������|�¼�|��������|�����¼|�ż���ַ
| �ײ� |
|
|
| �ز� |
|
|
�������ߣ� ��ά��˹����(David Stipp)
����һϵ���о��Ѿ�����������ҩ�����������һ����Ϯʮ����Ĺ��ϻ��ƣ���ȫ�п����ӳ������������ޣ���ֹ�ڶ����겡�ķ�����
����1964��11�µ�һ���峿�����ô�ʼҺ������Ӵӹ�������˹������ǰ���������ʼΪ��4���µĺ���̽�ա������̫ƽ���ϵ�һ����ɽ��������������2200Ӣ��(1Ӣ��Լ��1.6ǧ��)�������صľ���ͷ�����������������̽�յ�����Ǽ��ô�����ѧ��˹̹����˹������(Stanley Skoryna)��һλ�������ĵĿ�ѧ�ң�����һ����еĻ�������38λ��ѧ�ҡ����Ǽƻ������ƫԶ�ĺ�������һ���������о��������ִ�����������������Ͷ�ֲ�

��������ù����С��ʵ���еijɹ�������ζ��һ����ת������������ù�أ���û���κ�ҩ����������Ч���ӳ����鶯���������ޡ���������ҽѧ�����о���Ա���ⷽ���ͻ������������ˮ
����˹������һ�����ܵ����ؾ�������һ�ӭ��̽�ս��������Ǵ����������ֶ�ֲ��걾���Լ���������949λ�����ѪҺ����Һ�걾����ʵ���ϣ������ջ�����һ֧�Թ��е��������������к���һ��ϸ�����������ķ����Ի�ѧ������������ӳ�������ֵ�������
�������ֻ�ѧ���ʱ�����Ϊ����ù��(rapamycin)�����ʵ���ҵ��о�����ʾ����֮�����飬��ҩ��ȷʵ�ӳ���ʵ��С���������ޣ�������ƽ�����ޡ������������ʾij��ҩ���ӳ��˶����ƽ����������˵�����Կ�˥���Dz��ɿ��ģ���Ϊʹ�ÿ����ػ�����ҩ���ͨ�����ٹ����������ӳ�ƽ�����������ڿ�˥���ϲ�û�ж�����á��෴�������������(��Ⱥ������ٵ�10%�����ƽ������)�����ӻ�˥�ϵı�־����������ù�أ���û���κ�ҩ����������Ч���ӳ����鶯���������ޡ���������ҽѧ�����о���Ա���ⷽ���ͻ������������ˮ����ˣ������о�˥�ϣ��Լ����뷽�跨�Ը�˥����ؼ����Ŀ�ѧ����˵������ù����С��ʵ���еijɹ�������ζ��һ����ת������������������ҽѧ�Ҷ������ҵ�һ�ּ�ʩ���ӻ�˥�ϣ��ⲻ����Ϊ���ӳ�����������Ϊ����˥���ٶȣ������ӳٴӰ����ϵ���֢�ĸ������꼲���ķ���ʱ�䡣
����������������ҽѧ�Ҿ���������ɽ����������˥��ҩ���ϣ���������ǣ�������ã�����ſ�ѧ�ҷ����˿����ӳ����鶯��������Ļ���ͻ�䣬����������������Ϊ�����ӳ����ֶ�������������µ���ʶ����˥��ҩ��Ŀ����ƺ�����̹;һ��������չԶû������������˳������ѧ�һ�û���з����κ����ӳ����鶯���������ҩ���Ȼ�ڶ���ʵ���У�������������(��ʳ�����㹻��Ӫ���ɷ֣������������ϵ�)���������ӳ�С�������������ӳٰ�֢���������Լ�������������������ؼ����ķ��������Դ��������˵��ͨ���ϸ�Ľ�ʳ���ӻ�˥�ϲ������С�
����2006�꣬һ��С���о����֣�����е�һ����Ҫ�ɷְ�«��(resveratrol)�ܵ�����֬��ʳ������������̣�����Ч����һ���̶��������������ơ����ƺ���һ��ͻ�ƣ���ϧ���֤ʵ������������ȥ������øsirtuins�����ʻ��Dz����ӳ�������ʳС���������ޡ�Ȼ��������2009�����У�ʧ������Ӱһɨ���գ����������������о���(NIA)����������ʵ�������ϱ����ƣ�������ƽ��ʵ���У�����ù��(��ʱ�Ѿ�֪�����������ʾ�������ϸ������������)��ʹС�����������ӳ�12%�����ң��о���Ա����ط��֣�һЩ����������С����ҩ��ƽ������ھ�Ҳ�ӳ�������֮һ������ѧ�ұ�����Ϊ���ⲿ��С����ܶ�ҩ�ﲻ��Ӧ��
��������ù��ͻ���˲��鶯����������ޣ���ʹ��ѧ��ע�һ������Ѿ�������10������������ƣ��û����ƺ����Ե���С����������鶯���˥�Ϲ��̡��������������������Ҳ�������ࡣ��һ���Ƶĺ���Ҫ����TOR����(target of rapamycin��������ù�ص�Ŀ�군��)�Լ�����õ��Ļ���(TOR����)��TOR�����ǵ�������ҽѧ��ҩѧ���ص��ע������ΪԽ��Խ��Ķ��P�ٴ�ʵ����������Ʋ��鶯��ϸ���е�TOR����(��mTOR)�Ļ��ԣ��ܽ��Ͷ���������ؼ����ķ������գ����簩֢�������ĺ�Ĭ��������ɭ�����ļ������Բ��䡢���������������ɡ��ư߱��Եȡ�Ҳ����˵��ֻҪ�ҵ�һ��ҩ��ܰ�ȫ��Ч������mTOR���Ļ��ԣ���ô�������ӻ������˥�Ͻ��̣���������ù����С���е�����һ��������Ԥ��ҽѧ�����ż����ش������(��������ù�����ӳ�С���������ֵ����������ź����ǣ�����ù�ر����ĸ����þ���������������������)��
�����ڴ�֮ǰ����ѧ��Ҳ�����������������ӵ�ҩ�������������ر���sirtuins����ômTOR��������Щ������ʲô��ͬ������������mTOR����ҩ������Ч�ӳ����鶯���������ޣ��ⲻ��֤ʵ�ˣ�mTOR�����ڲ��鶯���˥�Ϲ��������Źؼ����ã�����Ҫ���ǣ��˵����ѧ�Ҽ���˥�Ͻ��̵����룬��ɹ��Ѿ�ǰ��δ�еؽӽ������ڽ����������10�꣬TOR�����ܶ��ǿ�ѧ������ϣ�����ڡ��������ܿ�ѷʵ���ҵ�����ҽѧ�ҡ�����ù��С��ʵ����о���֮һ���ġ����ջ�(Kevin Flurkey)˵��
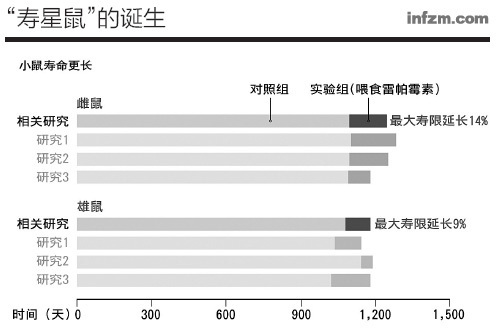
����2009�꣬����ƽ��ʵ��֤ʵ������ù�ؿ��Խ�С�����������ӳ�9%��14%��������������Ч�ӳ����鶯���������ҩ����ÿ�ѧ�ҿ������µ�ϣ�����о���һ�ּ���Ч��ҩ������ӻ������˥�Ϲ��̣��������˸�����������ù����Ϊ�����ã��ܿ��ܻᱻ�ų��ں�ѡ����֮��
��������˥��
�������꣬˹������̽�ջ����Ͱ����������ƽ�������������ҩ��(Ayerst)��ʵ���ң�TOR�ķ���֮��Ҳ�ɴ˿�ʼ��ֻ������������о����������TOR������˥�Ϲ����е����ã�����Ϊ�˿��������ء�����������40�������ҩ���̵��о���Աһֱ�������з���ϸ����Ѱ�ҿ����ء�
����TOR������Ӱ��˥�Ͻ��̵Ŀ�����Դ��20����90������ڵ�һϵ�з��֣�����״̬�£�ϸ���ή��TOR���Ļ��ԣ�����������������ʵ�ڴ�֮ǰ������ѧ�Ҿ��Ѿ��۲쵽���Ƶ�����1935�꣬�������ζ���ѧ��Ӫ��ѧ�ҿ��������(Clive McCay)���֣����������ʳ�﹩Ӧ����ʹ�����������������������ӳ��������Ժ��кܶ��о���֤ʵ�������������룬�����ӳ��ӽ�ĸ��֩�뵽���Ķ�����ֵ�������ޣ����ҳ����о����������ں�����Ҳ�����Ƶ�ЧӦ������������𣬺�Ӻ�ͼ�������֮һ���������룬��ʹ�����ӳ�30%��40%�������ϻ��õ����Զ��ƣ�ʹ�����Ӻ��ȥ�����������
��������������������������Ч��������Щʵ��С����������������̣�������֤�ݱ�����������������ȷʵ�����������˸�������������Щ��Ӻ�һ������ˣ������о������ϻ��Ŀ�ѧ����˵���ҵ�һ��ҩ��ڲ�������������ʳ������£��Ϳ����������꽡�������ã�������Ǵ�һ����
�����������ͳ�����ѧ�Ҷ�TOR�����˽��Ѿ��dz����룬�����Ʋ⣬���TOR������ϸ���е��������ã��Ϳ����������������Ƶ�Ч����2003�꣬��ʿ���ﱤ��ѧ�ķ���ѧ�ߡ���������ѧ�ҵٲ���ά��(Tibor Vellai)���о��߳�ʱ���õ�������TOR�����Կ�������˥�ϵ���֤�ݣ�ͨ������������ֹTOR���ĺϳɣ���ʹ�߳��ƽ�������ӳ�������һ���������������ѧԺ���˿�����������(Pankaj Kapahi)���֣�����TOR���Ļ���Ҳ���ӳ���Ӭ��ƽ��������������������������IJ���Ӱ�죬�����������������Ч��һ����2005�꣬��ʱ��ְ�ڻ�ʢ�ٴ�ѧ�IJ������������(Brian Kennedy)��ͬ�����о��У��ٴ�֤����TOR������˥�ϼ�Ĺ�ϵ��������Ͻ�ĸ��TOR�ź�ͨ·��ĸϸ���������ӳ��ˡ�
������Щ�Լ���������TOR�����о��ر����˸���Ȥ��ԭ���ǣ�����֤���ˣ�����TOR���Ļ��Բ��������������Ƶ�Ч����������ijЩͻ�����һ�����ӳ��������������Щͻ����������ν�ġ����ٻ���(gerontogene)���������������ʮ����ǰ�����ڻ׳����ڡ����������о������������ٻ������û���������ȵ����ź�ͨ·��˥��һֱ����Ϊ��һ�����˸��ӵĹ��̣�����������ȴ������ͨ���ı䵥�������ǿ��������ӻ�˥�Ϲ��̵ģ���Ϊҩ���ӻ�˥���ṩ�˿����ԣ�Ҳʹ����ҽѧ��Ϊһ���ȵ��о�������20��21����֮������ѧ������С������̷����˶��֡����ٻ������ǻ���������źţ��������ȵ����Լ����伫Ϊ���Ƶ�һ�ּ��ء����ȵ�������������1���������źš�2003�꣬һ��Я�������ٻ���С������˳��ټ�¼��������˽�5��ʱ�䣬��һ������£�ʵ����С����������ᳬ������롣��Щ�����ÿ�ѧ�Ҹ������ţ�˥���ǿ����ӻ��ġ�
�����������Ϊ��TOR���ס����������Լ������ٻ���Ĺ�������ʹ��ѧ�Ҽӿ첽����������ù�����ӻ����鶯��˥�Ͻ����ϵ�Ч������ʵ���ϣ�ֱ�������͵���10���Ҫ����ʱ������ѧ�Ҷ�û������Դ�TOR���ס��������ÿ���˹��ѧ�����ճ�����˥���о���������ҽѧ��ʷ���ġ���˹����(Steven Austad)˵��������Ϊ����ù�����������Ƽ������ڹ㷺ʹ�û�Բ��鶯������������á���������˹���µ�һλͬ������١���������(Zelton Dave Sharp)�ڻع���TOR��صĶ����о�֮��ȴ�����˲�ͬ���뷨��2004�꣬��������˵֮�£�һ�����С�����������о���չ�����������о��У�������Ա�᳤�ڸ�С��ιʳ����ù�ء�
����������������������������о����������о��������˿��ã���ΪС��ij��θ�ҩʱ��̫������С��20���´�ʱ�Ÿ�ҩ�������൱������60�ꡣ������ǰ���£���ʹ�����������룬Ҳ������Ч�ӳ�����С��������������ڵ�ʱ����û��һ������������ù�ػ������á�����˹����˵������2009�꣬�����о�ȴȡ������ʷ��ͻ�ƣ������о�����������ʵ���ҡ��������ճ�����˥���о��������ϡ�˹����(Randy Strong)ʵ���ҡ��ܿ�ѷʵ���ҵĴ�ά��E������ɭ(David E.��Harrison)�����Ъ����ѧ��������У������¡�A������(Richard A. Mille)ʵ�������ϱ���˵���������С����ȣ�����ù��ʹ��������ʹ���������ֱ��ӳ��˾��˵�28%��38%�����������ֱ��ӳ���9%��14%��
�������������˷ܵ��о�����֮��������ѧ��Ѹ�ٸ��������ǵ��о�Ҳ������TOR������˥�Ϲ����е���Ҫ���á�Ӣ���ش�ѧѧԺ�Ŀ�ѧ�ҷ��֣�һ����ΪS6K1�Ļ�����Ա���һ��ø������ǿmTOR�������ã�������Ƹû���ı������㲻�������꼲�����������Ҳ�õ��ӳ�(��ֵ��ǣ����ַ�������������������)�����⣬�״���С��ʵ����ȡ��ͻ�Ƶ�����������ʵ���һ����֣���С��9���´�ʱ��ʼιʳ����ù�أ�����20���´�ʱιʳ��Ч����ͬ����˵������ù����Ҫ�������ڷ������ã���������Ϊ�������ڣ�������ܿ�ʼ���ˣ��������������ù�ص����þ�����ֹ��Щ�����ķ�����
��������TOR���Ļ��Կ����ӳ�������ֵ������������о�˥�ϵĿ�ѧ�Ҷ��ԣ���һ��ʵ��������һƬ����������ͻȻ�����һյ���ơ��������Ⲣ����˵������˥����ص�ͨ·�Ͳ���Ҫ��ʵ���ϣ�����ҽѧ�����γ�����һ�ֿ���������������Ӱ�������;��������һ���ܸ��ӡ��кܶ��֧�����磬�������������ö��ַ������ԡ�У������ʹ�����˥�Ϲ��̲��������������������ɵ�Ԫ����һЩ�ȵ�����ص�ø�͵����ʣ��������ϸ���д���Ӧ����Ӧ��FoxO���ס����кܶ�֤�ݱ������ڲ��鶯���У�ȥ������ø���������������������Ƶ�ЧӦ��������ijЩ�����£��������������TOR���Ļ��ԡ������������ںܶද��(����Ҳ��������)�У�TOR�����ƺ������������ġ�CPU���������ۺϸ���������Ϣ�����ƻ����˥�����ʡ�
������������
�������о�TOR���ƺ��������ƺ����ӳ���ô�ද�������ʱ����ѧ��������һ�����ڴ��ڵ����⣺Ϊʲô����������һЩ�ֿ�˥�ϵĻ��ƣ�
��������������ý�������ѧ�Һ�ͷ�ۣ���Ϊ��һ�����ֵij�Ա������ʳ�ߡ���Ⱦ�������¹ʶ�ɥʧ����ʱ����Ȼѡ�������������������õط��ܺ������������������������������������Σ�գ����������������нϳ��Ĵ��ʱ�䣬������֮ǰ�л��ᷱ�ܺ������ɷ�ֳ�������������ڵı�Ҫ�Ծͻ����ۿۣ����ǻ���һ���������ľ�լһ��������Ѹ���˻������ǣ��������ƿ��ڶ�����ֵġ����ꡱʱ�ӳ����ǵ���������˵���÷���������һ�ֹ��϶����صĻ��ƣ����ֻ���Ӧ�����γ�����Ȼѡ������У��������ض��������ӻ�˥�ϡ�
���������������ì�ܵ�����һ�ֹ㷺�����Ľ����ǣ���ʳ��ȱ���ĽΣ�����������ٻᴥ��һ�ּ�����Ӧ���ж��������˥�Ͻ��̣���ʹ�����������ڻ�����תʱ��ɷ�ֳ����������˹����ȴ���Ͽ�����˵��������Ϊ����û��֤�ݱ���������������ٻ���Ұ����������ã���������ֻ����ʵ�����У��ڹ���ι���Ķ����п��Կ�����������ʹ��������������Ұ����������������ܿ���ȥ������û���ȵ��ӻ�˥�ϵĻ������ã����������Щ���������������һ�ּ�����Ӧ�����ˡ�
����һЩ����ҽѧ�Ҹ�������һ�ֽ����ƺ��������������������������һЩ������Ӧ����Щ��Ӧ�ڽ����г��ֵ�Ŀ����ʵ��˥���أ������ӳ�������һ�ָ���Ӧ���ѡ���˹������Ϊ����ʳ��ȱ����ʱ�ڣ�������Ĵ���ʳ������һЩ�dz���ʳ�����ܿ��ܻ�����������ʳ��û�еĶ��ء����ּ��ѵ���ʳ��Ϊ���ܴ�����һ�����ڵĶ��ط������ƣ���������Ϯ��ϸ���ͻ�����Ӧ�����ƺ����������������������ӻ���˥�ϡ�
��������ǰ��������˹���������˰�֢�о���(Roswell Park Cancer Institute)����������V��������˹��¡��(Mikhail V. Blagosklonny)������TOR��������о�������Ϊ��������֮���������Ч��������Ϊһ�������⡱��������˹��¡���Ƕ���˹��ѧ�ң��ڰ�֢�о���ϸ������ѧ����������㣬���Ŀ���Դ��һ������ì�ܵĹ۵㣺��������ʱ���ɻ�ȱ��������������������ȴ�Ὣ�����Ͻ���Ĺ������Ϊ���������ƻ��ӳ�������ԭ���ǣ�������˰������������Ĺ������;����������������;���У�TOR����������Ҫ��һ����
����������˹��¡��ĺ���˼���ǣ���Ϊ��������ֳ�Ĺؼ�Ҫ�أ�TOR�����������巢��������ƶ�˥�Ͻ��̡�һ���棬�����������źţ��������ڵ�ƽ����ϸ����ֳ(��������Ӳ���Ĺؼ�����)��֬������(�п����շ�ȫ������֢)���ȵ�������(����)���ƹ�ϸ������(�����ƻ�)��������������һ���棬���������������ã�ʹ�����ʺ����ܵ��������쳣�ۼ����ͷ����ɻ�����DNA�����ƻ�ϸ����������лϵͳ�����⣬��Ԫ�ڻ���һЩ���Խ���ĵ����ʾۼ���һ�𣬵��°����ĺ�Ĭ���ȶ����������Լ�����������˹��¡����о��Ѿ����������������ڣ�TOR���״��ݵ��ź��ܼ���ϸ��˥�ϣ���ͨ��ϸ���������������ڽ�ϸ����������֯��������������
��������������������˹��¡����Ϊ���ڽ��������У������岢û�в����ӻ�˥�ϵĻ��ƣ�����ù�ء��������ơ�����ͻ����ӳ����������������������Ȼ�緢�������⡪������ǡ�ø����˱�������˹��¡���Ϊ���쳣��������˥�Ϲ��̣�ʹ������������������ȡ�ʵ���ϣ���TOR�ź�ͨ·�����ֱ�����������������һ��˥�ϳ�������������֮����������Ϊ�˴ٽ����������ܲ�����˹��¡������ۺ���ӱ���������������۵����֮һ��ȴ��Դ��һ������Ϊ����֪�ļ�˵��1957�꣬�ѹʽ�������ѧ�����Ρ�����ķ˹(George Williams)�����˥������һЩ����˫�����õĻ����շ��������������ڣ���Щ������������а���������������ȴ��Σ����������˫������ܽ����������� ��Ϊ�����κ�ʱ��ֻҪ���������ͻ����Ȼѡ�������չ�����������ϵ�һ������������˹��¡����Ϊ��TOR�����������һ�֡�˫�����
����������������һ����������˹��¡�������Ҳ�������顣���ֿ�ѧ����Ϊ��������˹��¡��̫��ǿ��TOR�����ڴٽ������ϵ����ã������ǿ�����TOR�����������ã���������ϸ�������ɹ���(�ù��̻����ϸ�����)�����Ǹû����ƶ�˥�Ͻ��̵Ĺؼ����ء���������Щ��ѧ������Ϊ��������˹��¡������ۻ��DZȽϺ����ģ���������ѧ�Ļ�����˵����������˹��¡�Ṵ�ճ��˱��˶�û�����ľ�������������Ϊ��������ȷ�ġ���
����Ѱ������ġ�����ù�ء�
�������TOR������˥�ϵļ�������������ʲô�취��ֹ���������ã�����ù�ػ����ų����⣬��Ϊ�������صĸ����ã��������ߵ��̴�ˮƽ������ƶѪ���谭���������̡�
��������˫��(metformin)Ҳ����һ��ѡ������Ҫ�ܶ��о��������������á�����ҩ����õ���;�������������������˳��ڷ��ã��Խ���Ѫ��ˮƽ����Ȼ��������в����������ȷʵ�����TOR�ź�ͨ·��������һ����˥����ص�øAMPK(��������Ҳ���Լ����ø)���ٽ�ϸ����Ӧ����Ӧ����С��ʵ���У���ѧ�һ����֣�����˫���ڻ�������ϵ����ã��������������Ƶ�Ч��������һЩ֤�ݱ���������ҩ��Ҳ������������ද���������ޡ�Ҫ֪������˫�����������Ƿ�Ҳ���������������Ƶ�Ч�������ܻ��õȴ����ꡣ���ڣ���ѧ���������ϸ��С��ʵ�飬�����Ƿ������ӳ�������
��������ܴﵽ����ù����С���е�Ч������ô�˵�ƽ���������ӳ�5��10�꣬����һ���ܴ�Ľ�������Ϊ���ϸ������������ҵ��˿������Ѿ�����ʮ��Ľ�����Ҫ��ٳ߸�ͷ����һ�����ͻ����˶�Ա�������һ������ɼ�һ�����ѡ��������˵�ƽ��������20����������50%���ϣ����ڹ�ȥ10�ֻ꣬�����˲���2%(20���ͣ��й��˵�ƽ��������30������������2000���71.4�꣬��������100%�����ڱ�����ͷʮ�꣬��2000���71.4��������2009���73.05�꣬����Լ2.3%)�����������Ѿ������ܽ��������������������ʣ��ӳ�����ֻ�ܼ�ϣ���ڽ������겡�ķ����ʺ������ʣ������겡���Ʒ��õı�ըʽ����˵������ʵ����һ�����Ѷ������ǣ��ӻ�˥�ϵ�ҩ��ȴ����������һ�㣺�����൱��Ԥ����ҩ�������ֹ���ӻ�����մ����������ɡ������ϡ���֢������ή�������������������������꼲���ķ����ͷ�չ���������Ѫѹ��Ѫ֬��ҩ����Ԥ�����ಡһ����������ǵ�����������������һֱ����������ֱ����ȥ��
�����з���˥��ҩ�ﲢ�����ף�����һ���ϰ��������Կۺ����˵�˥���ٶȡ�����һ���õ����б��������ڿ�ѧ���ж�һ��DZ��ҩ�����Ч�ԣ������Ͳ����ڿ�չһ���ʱ�������ٴ�ʵ����������жϡ�������������Ѱ�Ұ�ȫ��Ч�Ŀ�˥��ҩ�ﶼֵ������Ϊ֮Ŭ������ʹ�����ӳ�������ֻҪ�ܸ��������˵Ľ�����Ҳ�ǹ���������
����˭���뵽��50��ǰ��һƿ������������������Ҫ���о��ɹ����������δ�����������Զ��Ӱ���أ�
����(Scientific American ���İ桶�����ѧ����Ȩ�Ϸ���ĩ��������ɾ�ڣ�����ΰ����跭��)
�ȴʣ�