| ������|�й��������̨|��վ��ͼ |
| �ͷ���Ϊ��ҳ |
��̸ | ֱ�� | �㳡 | ����ǽ | ���а�
• ���Ӵ��������ʶ�� • ���ؼ�ʮ����ȫ����
������Ŀ|
̽��������|
�ټҽ�̳|
������Ȼ|
����|
���
ԭ�����|��������|�����й�|��Ȼ����
��ѧ���磨��ͣ����| �ٿ�̽�أ���ͣ����| ���´��| �Ƽ�����
�߱��й�| �߽���ѧ| ��ɫ�ռ�| �Ƽ�֮��
�Ƽ�����| ��������| �л�����| ����
��֤������| ��֤��Ӱ��־| �ط�| ��֤������֮��
������| ������̸¼| ˿·����| �����DZ���
��������| �����ձ�| ��������| �����л���
�����й�| ����| ����֮��ɫ����| ��ת����
ֲ��|����|��ս|����|����|����|ʷ˵����|���ĵ���|�ܵ�|ʱ��|����̽��|�й��ʵ�|���պ���|��Ȥ|��ÿƼ�|�峯|��ʷʱ��|������|UFO|�Ļ�����|��¥��|����|����|�ղ�|��������|Ů��Ů��|Ů��|�Ƶ�|����|�˶�|��Դ����|����|��������|����|��������|����|��ʷ����|�ڽ�|����̽��|����|ר��|����|��ѧ̽��|�������|δ��֮��|����|����|����|���Ҵ�ʦ|����Ѱ��|��������|ս��|��Ȼ����|��ѧ|��������|�¼�|��������|�����¼|�ż���ַ
| �ײ� |
|
|
| �ز� |
|
|
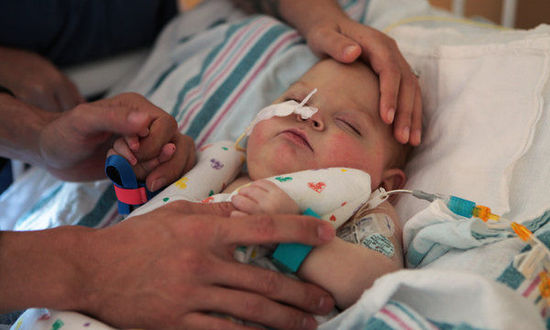
�������ˡ��ͷ����ʩ�ػ�����С�����г�������ҽ��Ŀǰ����Ѱ������������ٵķ����������о��Դ������ڽΡ�

�����ʩ��ҽ���Ϳ��������˶����ͷ����ʩ�ط��Լ����ǵĶ������ˡ�

�����������������ʩ��ҽ������ɼ����ͯҽԺ�����ҽ����������ʵ������о���Ա�������������С����֯��
������ɼ�������������������ʩ��ҽ��(Tracy Gritscht)���������г���һ��С������һ��һ�ε���ϸ��飬��ͬ�ڼ��һ��©�������г���̥һ����
�������С����һ����������һ��С�к����ˡ��ͷ����ʩ��(Mark Barfknecht)�����ڡ�����С�������˵ģ����ڸ�������������ɼ����ͯҽԺ������̨�ϵ�ԭ��������������£��ڳ���ʱ���ز���3������1.36�����Ӥ���У��ж��10%��Ӥ�����һ�ּ��������²��ֻ����ij���֯���������˾�������������������IJ�������أ��ֵ�С�����ѱ��г���
�����������ҽ�������ʩ������˼���ţ�����������ȶ���ʣ���С����
���������ʩ��ҽ�����ó����������������ġ��̳��ۺ�������������������Щ����ֻ�к��ٵ�С������������ʳ���˲��ò�ͨ������;�����Ӫ����
���������ʩ��ҽ��һ����������Ŭ�����Ȼ�����һ�滹�ھ����ҵ�һ�ֱȾ���Ӫ�����õĽ������������������п��������벻��������עӪ��Һ����ʱ�䣬��������ҽԺ�����ɳ���о�����(Saban Research Institute)ʵ������������о��Ŷ�һ��Ϊ�����������Ļ���Ѱ�ҹ������С���ķ���������Ҫͨ�����û��屾��ȥΪ��֯�ṩӪ�������ٽ���������
������ȫ������ع������������֯�����ٵ�ʵ����������ʩ��ҽ���������Ĺ����������ȵ�λ����Ȼ������������������ĸ������ٺ���֯���ֲ���ֲ��ȱ�ݣ�����Ȼ����һ�κܳ���·Ҫ�ߣ�����Ŀǰ�о������Ѿ��ɹ��ع�����������������ֽϼ����٣������������ʶ��ϸ�����ܹ�������ת��Ϊ��������ϸ���Ļ���ϸ��������Ľ�չ���Լ����¼����ķ�չ��
����Ŀǰ�����ʩ��ҽ�������������鶯��������������ʵ���������С����֯��������������ù���ϸ���ɹ����������������С����֯������ʼ�о���ο��������Ϊ���߷��˹����������أ�����������Ȼ��Ҫ�ü������ʵ�֣�������Ϊһ����ƴ���������������ɹ���
����������Ŀǰ����һ���ܴ�����⣬һ���ܽ��������⣬����ı�ܶ��ͯ��δ��������˵��
����������ʵ�����У������Ŷ�������������ʵ�顣�����Ƚ�����С���Ӷ�������ȡ�����жϣ���ø�����������ﴦ����ʹ���Ϊһ�Ż��ϸ��������һЩ��С���ڷ��ֵĸ�ϸ�������ǿ�ͽ����֯��ϸ����
������һ��ϸ������һ����Ŀ����オ������ϰ��ϣ���С����״������Ǧ���ϵ���Ƥ��������ϰ�䵱֧�ܵ����ã�֧�ֲ�����ϸ��������ʹ��ϸ�������������������֯������������
����������ҽѧ������֯���̣�����ϸ����ֲ��֧��������õķ����������ڴ����������£�Ŀ�������µ���������ȥ����������٣�����һ�����ܣ�����ԭλ�����µ�������֯��
���������ʩ��ҽ����ʵ�����гɹ�������һ���·������������������ʱ������������һ����ȥΪ���ṩӪ����
�������������Ŷӽ�һ��ϸ��ֲ������Ĵ���Ĥ����ǻ�ڵ�һ���۵����Ĥ״����ڴ���Ĥ�У�����ϸ�����ṩӪ������������Ѫ�ܰ�Χ��������ϸ������һ��������֯��ʱ�����ϰ����ձ����⡣����֮�����ʩ��ҽ���������о�Ա�ǽ���֯��Ӵ���Ĥ�з�����������ڸ��õ��о�������֯����������ġ�������֯����С�������гɷ֣�������Ƥϸ�������⡢��Ѫ�ܡ�
���������ڵ�����ʵ���У������ʩ��ҽ������һ����������֯ƴ�ӵ���С�����г��Ķ��������ϵͳ�С�ӵ������С���������û�е�����ָ��ø��졣
����ͨ����ʵ���ҹ���������ʵ����������������ʩ��ҽ������������Ϊһ�����ҽ��Ӧ�������¡������ƶ���ҽѧ�ķ�չ������˵��
��������40��ĸ����ʩ��ҽ���dz����飬������������ҽԺ�к������ϳ�����ӡ�в�ݮͼ������ñ�����������κ��ǽ��ⳤ��һֱϣ���Լ������Ϊһ�����ҽ������6�����꣬���Ͷ�����ĸ�������Լ���������롣��ҽʦѵ�������У����ܵ�С����Ƶ��������Ӷ�ѡ���Դ�Ϊ����ְҵ���������ȣ���ͯ�����������Ƶ���Ʒ������ʱ�������Ʒ��������ô���ƾ�����
������˵���������������Եĵط����ڣ���ν�һЩ�����Ǵ�����������һ�𣬲�ʹ�������������ȷ�Ľ������
������������һ�����ļ����ܹ���������ʵ���ң������߽������ҡ��ڽ���������С��������Ӥ����������С���������˵Ļ��ߣ����������г�С����������������һ������һ�ؽ�����С���͵��Աߵ����ϣ�������Ա�ܿ�������һ��ϸ��������ֲ�����ߵĴ���Ĥ�ϡ�
������С��ϸ��������ʱ���߿�����Ҫһ�������ҵľ���Ӫ�������ǵ�����֯�����ò��ɹ�ֲ���ʱ�����վͲ���Ҫ����Ӫ���ˡ�
������һ���̲�����Ҫ̫���µ�С��������ֻ��Ҫ����һ���ܹ��ֲ�ȱʧ�Ĺ��ܵ����٣��������ʩ��ҽ��˵����Ӣ��Ҳ�����㹻�ˣ������ʹ��ӵ���㹻�����չ��ܣ��Ӷ����Ѿ���Ӫ�������������������
�����������������Ʒ��������˶�����Ȼ̫��ңԶ��
�����������ٻص�������Щʱ�����һ�죬�������ң������ʩ��ҽ����������������������÷����ŵ˹(Demitri Merianos)ҽ������������˵�С������ʱ��û������С��С����֯�ļ��������Ǽ��о������������ܶ�������١�
���������ڵ�����խ�ĵط��ˣ��������ʩ��ҽ��˵�������������Ƕ���֯������������÷����ŵ˹ҽ�����˽�2Сʱ��ϸ�ش����˵ĸ�ǻ�������������֯������������ԭ�������ڸ����ϵ���֯��ʱ��һ���̴����Ƶĵ絶������
����Ϊ�˱�֤��4��Сʱ����������ʱ�������ܹ������˵ij�������ǡ���������������������������ߺͲ�ͬ�ļ��ӱ����С���Ŀ���ĩ�ˣ����������̽������˱ʼǡ�
��������Σ�С�������С��������ʩ��ҽ��������ü������÷����ŵ˹ҽ��һ����Ϊ���3Ӣ�糤��С�����뱻�г���
��������һ��ֻʣ15Ӣ�糤С����Ӥ����˵���ⲻ�Ǹ�����Ϣ��
����������ͬ��ĸ����˵��������һ���Ҵ��ߡ�
�������ǵģ����Ѿ����˺ܶ���ˣ����������ļ���Сʱǰ�����˵ĸ������˶�(Michael)������������Ӿ��ܵĸ���ĥ�ѣ��������迭������˵��������һ���������������ܼ��ˡ���Ը��Ϊ������һ�С���
����û����ȷ�е�֪����ʲô���¼���������������������е�һ�����ء�
�������ֽ��������Գ��ļ������ܹ���Ӥ�������������Ѹ�ٵػٻ�С�����ڴ�Լ�ķ�֮һ�IJ����У�С����֯�Ļ����������ġ��������ಡ��Ҳ��Ҫ���ܼ��������г�������֯�������ִ������µ����⡣
���������ҿ������ǵ�С��ʱ����֪��Ϊ��������ǵ�������Ҫ�г������С����֯���������ʩ��ҽ��˵�����������֯����������75%��Ӥ���������϶���Ҫͨ���������Ӫ���������������������˸��ࡣ������Ҫ��������С����ֲ���ڵ�������Ȼ�����ֻ�����µ����⡣
�������˺ܿ���75%����ֵ������������������ǰ��������ȥһ�������ӡ�ڰ������ļҽϽ�������һ��ҽԺ��ҽ�������������⾲��Ӫ����Ҳ����ȫ����Ӫ����total parental nutrition, ���TPN�����������ĸ����Ѿ���ʼ�ܵ����ˡ�
��������Ҫ��ǿ������Ϊ�˰ͷ����ʩ��������ȥ�˻�еʦ�Ĺ������������������˿���Ҫô��ҽԺ��Ҫô������Ժ�ȹ������ݵ�һ�������Ľ�㼸��û���������һ��
����������ϣ�����ؼң�������ĸ��˵��������ֻϣ�����ܻؼҡ���
������Ҳ�Ǹ����ʩ��ҽ����Ŀ�ꡣ���ǵ�����÷����ŵ˹ҽ����ȷ�������Ƿ����㹻��С�����հ��Ѿ���Ӫ��ʱ�����DZ��������Ѿ����ֵ���խ�������IJ��֡������ٴμ����һ�£�Ȩ����һ��ѡ�����Ƕ�β鿴���������̵��ϵıʼǡ�
�������治�ң��ټ��ɣ�����˵����ָ��÷����ŵ˹ҽ����ʼ�г�����С����
�������Ƕ����˶��ԣ���������һ������Ϣ�ˡ���ҽ�������鿴������С��ʱ�����Ǹ����ֹ۵���Ϊ���µ��ⲿ���Ѿ��㹻�ˡ�����һ�������ǻὫʣ�µij��ܷ������������ǻ���������ݺͽ᳦�������ӡ�������һ��ʱ��������Ҫ����ʹ�þ���Ӫ���������������ܹ�������ʳ��
����������Ϊ�����ܹ���������ȫ����Ӫ����Ȼ��������Իؼ��ˣ��������ʩ��ҽ��˵��
������Щ�������ܸ����������㹻�ij��ܣ�������Щ����ô���˵�Ӥ�������������ʩ��ҽ������Ϊ��������֯��Ŭ����
���������ҵĹ����У���Ϸ�����Ӥ����ȥ������˵�������룬��Ϊͬһ�����ⲻͣ�ô��Լ��Դ�����߶�š���̫����ˡ�����һ�����������Ƶ����顣��